免疫不全を伴うプロテアソーム関連自己炎症症候群(遺伝性の炎症性疾患)の発見とそのモデルマウスの樹立
生体が恒常性を維持するためには、不要あるいは合成不良のタンパク質が適切に分解処理されなければなりません。このタンパク質の分解処理に関わるタンパク質複合体(プロテアソーム*1)を構成するサブユニットタンパク質の遺伝子バリアント(遺伝子の違い)により、難治性の慢性炎症疾患(プロテアソーム関連自己炎症症候群)が発症します。今回、岐阜大学医学系研究科小児科学分野 大西秀典、和歌山県立医科大学先端医学研究所 改正恒康、邊見弘明(現在岡山理科大学獣医学部)、同大学皮膚科学 金澤伸雄(現在兵庫医科大学皮膚科学)、琉球大学小児科 金城紀子、長崎大学原爆後障害医療研究所 吉浦孝一郎、東京大学大学院薬学系研究科 村田茂穂、兵庫県立大学大学院理学研究科 水島恒裕らの研究グループは、プロテアソームサブユニットβ1iをコードする遺伝子(PSMB9)のde novo*2の新規のヘテロ接合性アミノ酸置換バリアントにより、免疫不全を伴うプロテアソーム関連自己炎症症候群という新たなタイプの遺伝性疾患が生じることを見出し、その病態を再現する新規のモデルマウスを樹立しました。
本研究成果は2021年11月24日(米国時間)に、国際誌Nature Communicationsに発表されました。
発表のポイント
- PRAAS*3様の炎症症状を新生児期に発症しながらも、通常のPRAASに認められる脂肪萎縮を示さず、また、PRAASではほとんど認められない肺高血圧やリンパ球減少を示す独立した2症例(琉球大学小児科、岐阜大学小児科)が見つかった。
- 詳細な遺伝子解析により、両患者において、プロテアソームサブユニットβ1iをコードする遺伝子(PSMB9)にde novoの新規のヘテロ接合性バリアント(β1iの156番目のアミノ酸であるグリシンをアスパラギン酸に置換させるバリアント、G156D)が病態の原因として有力な候補であることが示唆された。
- G156Dヘテロ変異マウスにおいて、患者由来の細胞での所見と同様のパターンで、β1iタンパク質の成熟、プロテアソームの構造および機能が障害されていた。
- G156Dヘテロ変異マウスを免疫学的に解析したところ、獲得免疫については、胸腺が萎縮すると共に、脾臓ではT細胞とB細胞いずれのリンパ球も減少し、抗体(免疫グロブリン)産生も顕著に低下しており、自然免疫については、樹状細胞が減少している一方で、好中球や単球は増加していた。
- G156Dヘテロ変異マウスに認められたプロテアソーム障害、免疫異常の表現型は、同変異を有する患者の所見と共通する部分が多く、G156D変異が患者の病態の原因であることが強く示唆された。
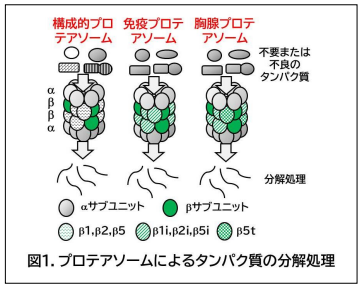
- *1 プロテアソーム:真核生物のすべての細胞に、構成的プロテアソーム、免疫プロテアソーム、胸腺プロテアソームのいずれかの形で存在している。構成的プロテアソームでは、タンパク質分解活性を担うサブユニットとして、β1、β2、β5が含まれているが、免疫プロテアソームでは、β1i、β2i、β5i、胸腺プロテアソームでは、β1i、β2i、β5tが含まれている。タンパク質が分解される際には、76個のアミノ酸から構成されるユビキチンが付加されるので、プロテアソームの機能低下により、細胞や組織にユビキチンが蓄積する。
- *2 de novo:ここでは、親から受け継いだ遺伝子バリアントではなく、患者に新たに生じた遺伝子バリアントであることを示す。
- *3 プロテアソーム関連自己炎症症候群(PRAAS):プロテアソームを構成するタンパク質の遺伝子バリアントを原因とする自己炎症性疾患の総称。1930年代から本邦で報告され、報告者である東北帝国大学皮膚科教授中條敦、和歌山県立医科大学皮膚科教授西村長應の名前を冠する、指定難病の中條・西村症候群はその一つであり、2011年に和歌山県立医科大学金澤、長崎大学吉浦、徳島大学安友らによって、プロテアソームサブユニットβ5iをコードする遺伝子(PSMB8)のホモ接合性バリアントを原因とする常染色体潜性(劣性)遺伝性疾患であることが明らかになっている。相前後して海外からも、β5iおよびそれ以外のプロテアソームサブユニットをコードする遺伝子のバリアントを原因とする症例が報告されている。
詳しい研究内容について
![]() 免疫不全を伴うプロテアソーム関連自己炎症症候群(遺伝性の炎症性疾患)の発見とそのモデルマウスの樹立
免疫不全を伴うプロテアソーム関連自己炎症症候群(遺伝性の炎症性疾患)の発見とそのモデルマウスの樹立
論文情報
- 雑誌名:Nature Communications
- 論文名:
Heterozygous missense variant of the proteasome subunit β-type 9 causes neonatal-onset autoinflammation and immunodeficiency. - 著 者:
Kanazawa N, Hemmi H, Kinjo N, Ohnishi H, Hamazaki J, Mishima H, Kinoshita A, Mizushima T, Hamada S, Hamada K, Kawamoto N, Kadowaki S, Honda Y, Izawa K, Nishikomori R, Tsumura M, Yamashita Y, Tamura S, Orimo T, Ozasa T, Kato T, Sasaki I, Fukuda-Ohta Y, Wakaki-Nishiyama N, Inaba Y, Kunimoto K, Okada S, Taketani T, Nakanishi K, Murata S, Yoshiura K, Kaisho T. - 論文公開URL:https://doi.org/10.1038/s41467-021-27085-y











